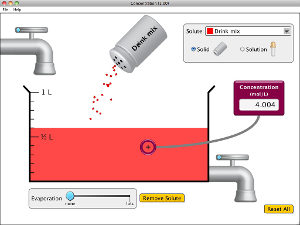
3. Propriétés des solutions
Concepts prescritsa. Solutions (sec 1)
i. Décrire les propriétés d’une solution aqueuse (ex. : une seule phase visible, translucide). b. Soluté (sec 3) i. Reconnaître le soluté dans une solution aqueuse donnée. c. Solvant (sec 3) i. Reconnaître le solvant dans une solution aqueuse donnée (ex.: lymphe, larmes, plasma cellulaire, urine) d. Concentration (sec 3) i. Définir le concept de concentration d'une solution ii. Décrire l'effet d'une variation de la quantité de soluté ou de solvant sur la concentration d'une solution. iii. Déterminer la concentration d'une solution aqueuse (g/L ou pourcentage). iv. Déterminer la concentration d’une solution aqueuse (g/L, pourcentage, ppm). (sec. 4) v. Déterminer la concentration d’une solution aqueuse (g/L, pourcentage, ppm, mol/L) (STE) e. Électrolytes (sec. 4) i. Définir le concept d’électrolyte. f. Force des électrolytes (STE) i. Associer qualitativement la force d’un électrolyte à son degré de dissociation. g. Échelle pH (sec. 4) i. Décrire l’échelle pH (acidité, alcalinité, neutralité, valeurs croissantes et décroissantes). ii. Déterminer le pH de quelques substances usuelles (ex. : eau distillée, eau de pluie, salive, jus de citron, produit nettoyant). h. Dissociation électrolytique (sec. 4) i. Décrire le processus de la dissociation électrolytique i. Ions (sec. 4) i. Définir le concept de ions j. Conductibilité électrique (sec. 4) i. Décrire le mécanisme permettant la conductibilité électrique dans une solution aqueuse (dissolution électrolytique d’un soluté, formation d’ions mobiles) Animations interactivesVidéos |
Notions |